باتری چیست ؟
باتری یا پیل الکتریکی (ولتاییک)، منبعی از انرژی پتانسیل الکتریکی است که در درون آن با انجام واکنشهای شیمیایی، انرژی شیمیایی به انرژی الکتریکی تبدیل میشود، این انرژی در قطبهای باتری قابل دریافت است.
انرژی قابل دریافت در قطبهای باتری به ازای واحد بار الکتریکی را نیرومحرکه الکتریکی (Electromotive force یا emf) باتری میگویند و آن را با یکای ولت اندازهگیری میکنند.
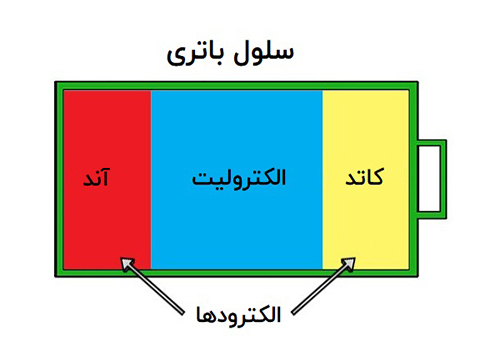
قطب مثبت را آند و قطب منفی آن را کاتد مینامند. (در فرهنگ عامیانه به قطبها، سر مثبت و سر منفی نیز گفته میشود.)
کارکرد باتری
معمولاً هر باتری از یک یا چند سلول کوچک داخلی تشکیل شده است.
در باتریها، ممکن است سلولها برای افزایش جریان با هم موازی شده یا برای افزایش ولتاژ با هم سری شوند.
هر سلول شامل دو نیم سلول است که به صورت سری، توسط مادهای الکترولیت -شامل یونهای مثبت و یونهای منفی – که رسانای الکتریکی میباشد به هم متصلاند.
با اتصال آن به مصرفکننده، یونهای منفی از طریق سیم هادی به مصرفکننده وارد میشوند.
بعد از ایجاد انرژی در آن (انرژی گرمایی بر اثر عبور از یک مقاومت یا انرژی جنبشی بر اثر القا یا انرژی نور بر اثر پرتاب و…) به سمت یونهای مثبت حرکت میکنند و به تدریج یونهای مثبت (که در اینجا حفرهها هستند) را خنثی میکنند.
با گذشت زمان یونهای مثبت بیشتری خنثی شده و به تدریج انرژی باتریها کم شده و مقاومت داخلی آن افزایش میباشد.
در این حالت بعد از گذشت مدت زمانی که معمولاً با آمپر ساعت باتری مشخص میشود.
باتری به صورت کامل تخلیه میشود. مثلاً یک باتری ۶۰ آمپر ساعت میتواند ۶۰ آمپر را تا یک ساعت تأمین کند.
این باتری بعد از گذشت یک ساعت و با کشیدن جریان ۶۰ آمپر از ان به صورت کامل تخلیه میشود.
با کاهش جریان دریافتی میتوان مدت زمان کارایی آن را افزایش داد، در این حالت باید پارامترهای مانند دما، لزرش و مقدار تنش موجود در جریان را نیز در زمان نهایی لحاظ کرد.
به عنوان مثال باتری ۶۰ آمپر ساعتی در حالت تئوری باید جریان ۲۰ آمپر را برای مدت زمان ۳ ساعت تأمین کند .
در حالی که با توجه به ساختار باتری و همچنین دمای محیط ممکن است این زمان تا نیم ساعت نیز کاهش یابد.
تقسیمبندی باتریها
از بالا به پایین: یک باتری ۴٫۵ ولتی و D Cellو یک C cellو یک AA cell و یک AAA cell و یک AAAA AAAA cell و یک A23 battery و یک ۹-volt PP3 battery و یک جفت باتری CR2032 and LR44.
بر اساس شرایط محیطی و شرایط الکتریکی مورد استفاده بایستی از باتریهای متفاوت استفاده نمود. باتریهایی که دارای مشخصات گوناگون تحت شرایط دشارژ میباشند.
انواع باتری از نظر کاربرد
انواع باتری از نظر کاربرد عبارت اند از:
- خورشیدی که شارژ آنها تابع قوانین خاص است.
- باتریهای مورد استفاده در ups و لپتاپ و موبایل، که توانایی تأمین یک جریان ثابت برای مدت زمان طولانی را دارند.
- باتریهای اتومبیل، لیفتراک و موتورسیکلت، که میتوانند جریان زیادی را در مدت زمان کوتاه جهت استارت تأمین کنند.
- باتریهای سامانههای حفاظتی، روشنایی، امنیتی و سامانههای کنترل، که باید دارای عمر و پایداری بالایی باشند.
- قلمی و نیم قلمی و…، که برای مصارف عمومی ساخته شدهاند و این باتریها باید ارزان باشند.
- سکهای و باتریهای پشتیبان، که میتوانند جریان کمی را برای مدت زمان خیلی طولانی تأمین کنند.
و…بطور کلی باتریها به دو دسته قابل شارژ و غیرقابل شارژ تقسیمبندی میشوند.
باتریهای شارژ نشدنی (یک بار مصرف)
این باتریها قادر به شارژ الکتریکی نبوده و یکبار استفاده و شارژ میشوند و معمولا سلولهای خشک (باتری خشک) نیز نامیده میشوند.
در باتری خشک معمولی، بر اثر واکنش ماده آند (قطب مثبت) (عنصر Zinc یا Alkaline یا Lithium یا Silver)و ماده کاتد (قطب منفی) (عنصر carbon یا chloride یا copper oxide یا iron disulfide یا manganese dioxide) با الکترولیتی که محیط بین آند و کاتد را دربر گرفتهاست،
انرژی شیمیایی به انرژی الکتریکی تبدیل میشود.
اساس نامگذاری باتری با نامهای همچون باتری لیتیوم (Lithium) یا باتری Alkaline یا …، به دلیل عناصر استفاده در ساخت آنها است.
در جدول زیر توضیحات بیشتری آورده شده است:
| ساختار شیمیایی | ولتاژ نامی هر سل | انرژی ویژه | نمونه و کاربرد ویژگی |
|---|---|---|---|
| Mercury oxide | ۱٫۳۵ | قابلیت تأمین ولتاژ و جریان ثابت، این باتری به دلیل مضر بودن Mercury oxide برای سلامتی تولید نمیشود . |
|
| Zinc–air | ۱٫۳۵–۱٫۶۵ | ۱٫۵۹ | قیمت بالا، قابلیت پیادهسازی در ابعاد بسیار کوچک – قابل استفاده در دستگاههای کوچک نظیر ساعت مچی و سمعک. |
| Alkaline (zinc–manganese dioxide) | ۱٫۵ | ۰٫۴–۰٫۵۹ | قیمت بالا، قابلیت پیادهسازی در ابعاد بسیار کوچک – قابل استفاده در دستگاههای کوچک نظیر ساعت مچی و سمعک. |
| Lithium (lithium–iron disulfide) LiFeS۲ | ۱٫۵ | قیمت زیاد، مناسب برای سیستمهای گرانقیمت و حساس، نظیر ریموتهای کنترل، دوربین و … . |
|
| Zinc–carbon | ۱٫۵ | ۰٫۱۳ | کاربردهای عمومی (باتری ارزان). |
| Zinc–chloride | ۱٫۵ | کاربرد عمومی با عمر بیشتر نسبت به Zinc–carbon. |
|
| Silver-oxide (silver–zinc) | ۱٫۵۵ | ۰٫۴۷ | قیمت بسیار بالا، از پایداری بالای برخودار است و از آن در دستگاههای تجاری و نظامی برای تغذیهٔ پشتیبان میکروکنترلرها و cpu ها استفاده میشود . |
| Lithium (lithium–copper oxide) Li–CuO | ۱٫۷ | دیگر تولید نمیشود. با باتری silver oxide (IEC-type “SR”) جایگزین شدهاست. |
|
| Nickel oxyhydroxide (zinc–manganese dioxide/nickel oxyhydroxide) | ۱٫۷ | ظرفیت انرژی متوسط، مناسب برای مقاصد تمیز (باتری نشتی ندارد). |
|
| Lithium (lithium–manganese dioxide) LiMnO۲ | ۳٫۰ | ۰٫۸۳–۱٫۰۱ | قیمت زیاد، عمر طولانی، مناسب برای تغذیهٔ سیستمهای پشتیبان، جریان نشتی داخلی کمی دارد و میتواند جریان کمی را برای مدت زمان طولانی تأمین کند. |
هر باتری یک مقاومت داخلی (R) دارد و اختلاف پتانسیل بین قطبهای باتری (V)، زمانی که جریان I از آن میگذرد، برابر V=Eemf – IxR میباشد.
فرایند تبدیل انرژی، باعث افزایش مقاومت الکتریکی داخلی آن میشود و این حالت تا آنجا پیش میرود که نیرومحرکه، دیگر توانایی غلبه بر آن را نداشته باشد.
افزایش مقاومت الکتریکی به دلیل نفوذ مادهٔ کاتد (منفی) به داخل مادهٔ آند رخ میدهد.
در برخی از مواقع، میتوان با گرم و سرد کردن باتری (انداختن در آب جوش و منقبض و منبسط کردن باتری) یا زدن ضربه، مسیرهای جدیدی را برای عبور جریان ایجا کرده و مقاومت R را تاحدودی کم کرد.
در باتری فرسوده مقاومت داخلی به قدری زیاد است که با عبور جریان، ولتاژ دو سر باتری به سرعت افت میکند و باتری قابلیت تأمین انرژی الکتریکی مفید را ندارد.
[adinserter name=”Block 2″]
باتریهای شارژشدنی
توجه داشته باشید که برای اطلاعات بیشتر میتوانید به بخش باتری قابل شارژ مراجعه کنید.
از این باتریها برای مقاصد زیر استفاده میشود:
باتریهای نیروگاهی (GROE-OGI-OPZS-FNC)
باتریهای آنتنهای مخابراتی باتریهای مخابراتی NET Power-power
باتریهای مورد استفاده در سامانههای ریلی و مترو
باتریهای مورد استفاده در پروژههای نفت، گاز و پتروشیمی (FNC)
باتریهای خورشیدی (Solar.bloc)
باتریهای مورد استفاده در ups
باتریهای منابع تغذیه (SLA – VRLA)
باتریهای اتومبیل، لیفتراک و موتورسیکلت
باتریهای سامانههای حفاظتی، روشنایی، امنیتی و سامانههای کنترل
این باتریها پس از دشارژ، با عبور جریان در جهت مخالف جریان دشارژ، به صورت الکتریکی قابل شارژ هستند.
با نام باتریهای ذخیره یا شارژی نیز شناخته میشوند و عمر این باتریها، بیشتر از ۵ سال است و بارها میتوان آنها را شارژ و دشارژ کرد.

کاربردهای باتریهای شارژشدنی
۱ – کاربردهایی که به دلیل صرفه اقتصادی و نیاز به توان بالاتر از توان باتری غیرقابل شارژ:
در این موارد هر چند امکان استفاده از باتریهای غیرقابل شارژ نیز وجود دارد ولی هزینه زیاد، کارائی کم و آلودگی محیط زیست را در پی خواهد داشت.
۲ – کاربردهایی که در آنها از باتریهای قابل شارژ به عنوان وسیله ذخیره انرژی استفاده میشود:
در این گونه فعالیتها، باتریها توسط یک منبع انرژی اولیه شارژ و در هنگام نیاز انرژی ذخیره شده را به بار تحویل میدهند.
در این حالت، باتری همیشه توسط یک شارژر در زیر شارژر قرار گرفته است و در مواقع قطع برق، انرژی مورد نیاز مصرفکننده را تأمین میکند.
باتری منبع تغذیه بدون وقفه و باتری اتومبیل، لیفتراک و موتورسیکلت، نمونهای از این کاربرد میباشد.
انواع باتریهای قابل شارژ
باتریهای قابل شارژ را میتوان به دو دسته کلی اسیدی و بازی تقسیمبندی نمود. باتریهای قابل شارژ براساس جنس الکترودهای مثبت و منفی، به انواع گوناگون تقسیمبندی میشوند.
برای کاربردهای صنعتی ساکن، در اکثر موارد از باتریهای نیکل–کادمیوم (بازی) و برای کاربردهای که در آن لرزش وجود دارد معمولاً از باتری سرب – اسید استفاده میگردد.
از ویژگیهای باتریهای قابل شارژ، علاوه بر قابلیت شارژ مجدد، توان بالا، نرخ دشارژ سریع و مشخصه عملکرد بهتر دمای پائین میباشد.
باتری نیکل – کادمیوم را معمولاً در Battery room یا باتری خانه نگهداری میکنند.
توان الکتریکی باتری
توانی که هر باتری بر حسب وات فراهم میکند، برابر حاصلضرب ولتاژ آن (بر حسب ولت) در حداکثر جریان مجاز آن (برحسب آمپر) میباشد.
در کاربردهایی با توان بالا، از جمله راه اندازه موتور خودرو، میزان توانهای تأمین شده در فواصل زمانی کوتاه به بیش از ۱۰۰۰ وات میرسد.
در کاربرد کم توان در وسایل الکترونیکی ظریف، مانند سمعکها و ساعتهای رایانهای، اندازه توانهای فراهم شده نزدیک چند میلی وات است.
خطرات و نقایص
خطرها و نقصهای مربوط به باتری عبارتند از:
انفجار (پدیده انفجار باتری عموماً ناشی از عدم کاربرد یا کارکرد صحیح باتری است.)
نشتی
ملاحظات زیستمحیطی
به عنوان مثال تلاش برای شارژ نمودن مجدد باتریهای یک بار مصرف یا غیرقابل شارژ، اتصال کوتاه نمودن دو قطب مثبت و منفی باتری میتواند باعث انفجار این منبع انرژی الکتریکی شود.
نشت مواد شیمیایی
در بعضی از باتریها از مقوا، فلز روی و مواد شیمیایی استفاده میشود.
واکنش شیمیایی درون باتری در مدت زمان طولانی، باعث خروج و نشت مواد شیمیایی داخل باتری به بیرون میشود.
همچنین، باعث ایجاد خوردگی شیمیایی در قطعات فلزی دستگاهها ( که اطراف باتری قرار دارند)، میشود.
ملاحظات زیستگاهی
افزایش بهرهگیری از باتریها و کاربردهای گسترده آن، افزایش زبالههای صنعتی و زیستگاهی تازه این کالا را به همراه داشتهاست.
تولیدکنندگان باتری، از مواد شیمیایی خطرناک، برای بالابردن کارایی باتریهای ساخته شده خود، سود میجویند.
البته امروزه پژوهشگران زیادی در تلاش بوده تا این خطرات را ( با ساخت باتریهای چندبار مصرف که باعث کاهش زبالههایی از این قبیل میشود)، کاهش دهند.
تاریخ نخستین باتریها
پیل الکتریکی در ایران باستان در فاصله سالهای ۲۵۰ ق. م تا ۲۲۴ پ. م در تیسفون ساخته شد.
این باتریها به باتریهای بغداد و پیل الکتریکی مشهورند.
شرکت جنرال الکتریک این باتریها را با روش تاریخگذاری رادیوکربن (به انگلیسی: Radiocarbon dating) شبیهسازی کردهاست.
معلوم شدهاست که قدمت این پیلها به ۲۰۰ سال پیش از میلاد میرسد.
.این پیلها دارای بدنهٔ بیرونی از جنس ارتن ور بوده که حاوی میلهای آهنی است
.این پیلها به وسیلهٔ بخشی از بدنهٔ مسی (میلهٔ آهنی درون استوانهٔ مسی) ایزوله شده است
زمانی که درون محفظه با محلولی الکترولیت مانند آبلیمو پر شود، این وسیله جریان الکتریکی خفیفی تولید میکند.
این احتمال وجود دارد که این وسیله برای آبکاری الکتریکی جواهر به کار میرفته است.
اکتشافات باستان شناسان در مورد باتریها
در سال ۱۳۱۷ خورشیدی برابر با ۱۹۳۸ میلادی، باستانشناس آلمانی ویلهلم کونیک، ابزارهایی را در نزدیکی تیسفون پایتخت ایران، در دوران اشکانیان یافتند.
پس از بررسی معلوم شد که این ابزارها پیلهای الکتریکی هستند که در دوره تاریخی ایران اشکانی ساخته شده و به کار میرفته است.
او، این پیلها را، باتری پارتی یا باتری باستانی نامید.
امروزه این پیلها، با نامهای دیگر، همچون باتری پارتیان یا پیل اشکانی هم مشهورند.
وسیله ای که برای آبکاری الکتریکی و انتقال لایهای از طلا یا نقره از سطحی به سطح دیگر به کار میرفته است.
تئوریها و فرضیههای مختلف در مورد اکتشافات باستان شناسان
این اکتشاف مربوط به دوره تاریخی سلسله اشکانیان، تاحدی موجب شگفتی است.
حتی برخی از دانشمندان اروپایی و آمریکایی این باتری را به موجودات فضایی افسانهای نسبت دادند.
عدهای هم معتقد بودند، احتمالاً ساکنان فراهوشمند سیارات دیگر که با بشقابهای پرنده به زمین آمده بودند، این باتریها را درست کردهاند!
آنها، آن را فراتر از دانش اندیشمندان و پژوهشگران آن دوران دانستند.
برای ایشان پذیرفتنی نبود که دانش ایرانیان در آن زمان تا به این حد بالا باشد.
۱۵۰۰ سال پیش از گالوای ایتالیایی(۱۷۸۶ میلادی)، که پیل الکتریکی را اختراع نمود.
احتمالا ساکنان بینالنهرین از این پیلهای الکتریکی جریان برق تولید میکردند و از آن برای آبکاری اشیاء زینتی، سود میجستند.
اما در پهنه دریانوردی منطقه خاورمیانه، از این اختراع، جهت آبکاری ابزارهای آهنی در کشتی و جلوگیری از زنگ زدن و تخریب آنها استفاده میشده است.
این تئوری، بعدها توسط دانشمندان دیگری به بوته آزمایش سپرده شد.

بازسازی باتریهای تاریخی
ویلارد گری، مهندس برق شرکت جنرال الکتریک در ایالت ماساچوست، پس از مطالعهٔ مقالهٔ کونیگ، تصمیم گرفت باتری بغداد را بازسازی کند.
وی درون کوزهٔ سفالین را با آب انگور، سرکه یا محلول سولفات مس پر کرد و موفق به تولید ولتاژ حدود ۱٫۵ تا ۲ ولت شد.
بعدها دکتر اگبرشت، مصرشناس مشهور در سال ۱۹۷۸ نمونهای از باتریهای بغداد را بازسازی کرد .
اگبرشت، آن را با آب انگور پر نمود و توانست ولتاژ ۰٫۸۷ ولت تولید کند.
وی از این پیلها، برای طلاکاری یک پیکرهٔ نقرهای استفاده کرد.
نمونههای بیشتری از این باتریهای باستانی در سال ۱۹۹۹ توسط دانشجویان دکتر Marjorie Senechal، استاد ریاضیات و تاریخ علم در Smith College ماساچوست، ساخته شد.
آنها با پر کردن کوزهٔ آن با سرکه، قادر به تولید ولتاژ ۱٫۱ ولت بودند.
علاوه بر تئوری استفاده از این باتریها برای آبکاری الکتریکی فلزها، تئوریهای دیگری مبنی بر استفادهٔ پزشکی یا موارد دیگر داده شده است.